Содержание
Дегидроэпиандростеронсульфат (ДЭА-SO4)
Дегидроэпиандростеронсульфат (ДЭА-SO4) – это андроген, мужской половой гормон, который присутствует в крови как у мужчин, так и у женщин. Он играет важную роль в развитии вторичных мужских половых признаков при половом созревании и может преобразовываться в тестостерон и эстрадиол. ДЭА-SO4 вырабатывается корой надпочечников, его производство контролируется адренокортикотропным гормоном (АКТГ).
Женщинам рекомендуется сдавать анализ на 8-10-й день цикла.
Синонимы русские
Дигидротестостерон сульфата, ДЭА-С.
Синонимы английские
Dehydroepiandrosterone Sulfate, 5-Dehydroepiandrosterone (5-DHEA).
Метод исследования
Конкурентный твердофазный хемилюминесцентный иммуноферментный анализ.
Диапазон определения: 0,1 — 5000 мкг/дл.
Единицы измерения
Мкг/дл (микрограмм на децилитр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 2-3 часов перед исследованием, можно пить чистую негазированную воду.
- Прекратить прием стероидных и тиреоидных гормонов за 48 часов до исследования (по согласованию с врачом).
- Исключить физическое и эмоциональное перенапряжение за 24 часа до исследования.
- Не курить в течение 3 часов до исследования.
Общая информация об исследовании
Дегидроэпиандростеронсульфат – это мужской половой гормон (андроген), который содержится в крови как мужчин, так и женщин. Он участвует в формировании мужских вторичных половых признаков во время полового созревания и может быть преобразован организмом в более действенные андрогены (тестостерон и андростендион), а также конвертирован в женский гормон эстроген. Выработка ДЭА-SO4 контролируется питуитарным адренокортикотропным гормоном (АКТГ), а также другими питуитарными факторами.
Дегидроэпиандростеронсульфат является информативным маркером функции надпочечников. Опухоли и рак надопочечников, а также их гиперплазия могут привести к избыточному производству ДЭА-SO4. У мужчин повышение уровня этого андрогена иногда остается незамеченным, в то время как для женщин оно опасно аменореей и маскулинизацией.
Избыточное производство ДЭА-SO4 у детей способствует преждевременному половому созреванию у мальчиков и неоднозначным наружным половым органам, повышенному оволосению тела и аномальным менструальным циклам у девочек.
Для чего используется исследование?
- Для оценки функции надпочечников.
- Для того чтобы отличить болезни, связанные с надпочечными железами, от заболеваний, вызванных нарушением функций яичников и тестикул.
- Для помощи в диагностике опухолей коры надпочечников, рака надпочечников, врождённой либо приобретенной гиперплазии надпочечников и для отличия этих заболеваний от опухолей и рака яичников.

- Для помощи в диагностике синдрома поликистозных яичников.
- Для выяснения причин бесплодия, аменореи и гирсутизма.
- Для диагностики и выяснения причин маскулинизации у девочек, а также преждевременного полового созревания у мальчиков.
Когда назначается исследование?
- Как правило, совместно с тестами на другие гормоны при подозрении на избыток (редко на недостаток) образования андрогенов либо при необходимости проверки функционирования надпочечников.
- При симптомах аменореи, бесплодия или маскулинизации у женщин. В последнем случае имеются такие признаки, как низкий голос, гирсутизм (избыточный волосяной покров), облысение по мужскому типу, угревая сыпь, увеличенный кадык, маленькая грудь, у девочки – неоднозначные гениталии, когда клитор вырастает очень большим, в то время как внутренние женские органы выглядят нормальными.
- Когда у маленьких мальчиков происходит преждевременное половое развитие: слишком рано голос становится низким, появляются волосы на лобке, развивается мускулатура и увеличивается в размерах пенис.

Что означают результаты?
Референсные значения
|
Возраст
|
Референсные значения
|
|
Дети
| |
|
108 — 607 мкг/дл
| |
|
1-4 недели
|
31,6 — 431 мкг/дл
|
|
1-12 месяцев
|
3,4 — 124 мкг/дл
|
|
1-5 лет
|
0,47 — 19,4 мкг/дл
|
|
5-10 лет
|
2,8 — 85,2 мкг/дл
|
|
Женщины
| |
|
10-15 лет
|
33,9 — 280 мкг/дл
|
|
15-20 лет
|
65,1 — 368 мкг/дл
|
|
20-25 лет
|
148 — 407 мкг/дл
|
|
25-35 лет
|
98,8 — 340 мкг/дл
|
|
35-45 лет
|
60,9 — 337 мкг/дл
|
|
45-55 лет
|
35,4 — 256 мкг/дл
|
|
55-65 лет
|
18,9 — 205 мкг/дл
|
|
65-75 лет
|
9,4 — 246 мкг/дл
|
|
> 75 лет
|
12 — 154 мкг/дл
|
|
Мужчины
| |
|
10-15 лет
|
24,4 — 247 мкг/дл
|
|
15-20 лет
|
70,2 — 492 мкг/дл
|
|
20-25 лет
|
211 — 492 мкг/дл
|
|
25-35 лет
|
160 — 449 мкг/дл
|
|
35-45 лет
|
88,9 — 427 мкг/дл
|
|
45-55 лет
|
44,3 — 331 мкг/дл
|
|
55-65 лет
|
51,7 — 295 мкг/дл
|
|
65-75 лет
|
33,6 — 249 мкг/дл
|
|
> 75 лет
|
16,2 — 123 мкг/дл
|
Приемлемые уровни ДЭА-SO4 и других андрогенов могут свидетельствовать о нормальном функционировании надпочечников. Гораздо реже количество ДЭА-SO4 бывает в норме при опухоли надпочечника, но при этом не происходит секретирования гормона. При синдроме поликистозных яичников уровень ДЭА-SO4 может быть как повышенным, так и нормальным, поскольку это заболевание обычно связано с производством андрогенов яичниками (главным образом тестостерона).
Гораздо реже количество ДЭА-SO4 бывает в норме при опухоли надпочечника, но при этом не происходит секретирования гормона. При синдроме поликистозных яичников уровень ДЭА-SO4 может быть как повышенным, так и нормальным, поскольку это заболевание обычно связано с производством андрогенов яичниками (главным образом тестостерона).
Повышенный уровень ДЭА-SO4 может свидетельствовать об опухоли коры надпочечников, раке либо гиперплазии надпочечников. Он не является диагностическим признаком какой-то определенной болезни, однако указывает на необходимость дальнейшего обследования для выявления причин гормонального дисбаланса.
Низкий уровень ДЭА-SO4 бывает вызван дисфункцией надпочечников или гипопитуитаризмом, нарушениями, являющимися причиной понижения уровня питуитарных гормонов, которые, в свою очередь, регулируют производство и секрецию гормонов, производимых надпочечниками.
Что может влиять на результат?
- У новорождённых детей уровень ДЭА-SO4 обычно высокий.
 Он резко падает после рождения и затем возрастает при половом созревании. Пика концентрация ДЭА-SO4 достигает после полового созревания, затем она уменьшается с возрастом.
Он резко падает после рождения и затем возрастает при половом созревании. Пика концентрация ДЭА-SO4 достигает после полового созревания, затем она уменьшается с возрастом. - Прием дегидроэпиандростеронсульфатных добавок приводит к повышенному содержанию этого гормона в крови.
Сдать анализ крови на ДГЭА-С в Москве по доступной цене
ДГЭА-С — андроген слабо выраженного действия, образуется преимущественно в коре надпочечников (95%). ДГЭА-С обладает умеренным анаболическим действием, отвечает за развитие половых признаков и поддержание половых функций. Измерение ДГЭА-С в сыворотке крови позволяет оценить синтез андрогенов надпочечниками, особенно у женщин при повышенном уровне тестостерона для уточнения локализации источника андрогенов.
Уровень ДГЭА-С может резко возрастать при андрогенпродуцирующих опухолях (совместно с тестостероном).
Данный тест чаще всего назначают при гиперандрогениях вместе с 17-ОН-прогестероном для исключения врожденной дисфункции коры надпочечников.
ДГЭА-С – это андроген (мужской половой гормон), который присутствует в организме представителей обоих полов. У мальчиков в пубертатном периоде он отвечает за развитие вторичных половых признаков. Гормон способен преобразоваться в эстрадиол, андростендион и тестостерон. Его синтез проходит под контролем АКТГ и других факторов.
Уровень гормона служит достоверным показателем функционирования надпочечников. При наличии злокачественных или доброкачественных новообразований часто становятся причиной повышения синтеза этого гормона. Также высокие показатели характерны для гиперплазии надпочечников. У мужчин чрезмерное количество гормона во многих случаях никак не проявляется и остается незамеченным. У представительниц женского пола его чрезмерная выработка чревата аменореей и появлением признаков маскулинизации.
Для детей повышение продукции гормона чревато серьезной опасностью. У мальчиков оно вызывает чрезмерно ранее половое созревание. Если ДГЭА-С синтезируется слишком много в организме девочки, возможно нарушение менструального цикла, появление избыточного оволосения. Наружные половые органы приобретают неоднозначный внешний вид.
Наружные половые органы приобретают неоднозначный внешний вид.
Результаты анализа крови на ДГЭА-С используются врачом, чтобы оценить функционирование надпочечников. Также тест проводится для дифференциаций заболеваний, которые связаны с надпочечниками, от патологий, вызванных нарушением функционирования тестикул и яичников. В ходе диагностики новообразований коры надпочечников доброкачественного и злокачественного характера, гиперплазии, тест назначают в комплексе с другими анализами и инструментальными тестами. По полученным результатам можно отличить заболевания надпочечников от онкологии яичников и их доброкачественных новообразований. Тест также назначается, чтобы установить причину аменореи, бесплодия, гирсутизма, преждевременного полового созревания у мальчиков и маскулинизации у девочек.
Нормальный уровень андрогенов, как правило, указывает на то, что функционирование надпочечников не нарушено. При наличии новообразований надпочечников концентрация гормона обычно повышена, но иногда она может оставаться в пределах референсных значений. У пациентов с синдромом поликистозных яичников синтез гормона может повышаться или оставаться нормальным.
У пациентов с синдромом поликистозных яичников синтез гормона может повышаться или оставаться нормальным.
Повышенные показатели характерны для ряда заболеваний, поставить точный диагноз по результатам одного теста невозможно. При выявлении нарушений проводится комплексное обследование. Недостаток гормона также может указывать на различные патологии (например, он характерен для гипопитуитаризма). Референсные значения зависят от возраста и пола пациент.
Дегидроэпиандростерон Информация | Mount Sinai
Alhaj HA, Massey AE, McAllister-Williams RH. Влияние введения ДГЭА на эпизодическую память, кортизол и настроение у здоровых молодых мужчин: двойное слепое плацебо-контролируемое исследование. Психофармакология (Берл). 2006;188(4):541-551.
Андус Т., Клебл Ф., Роглер Г., Брегенцер Н., Шольмерих Дж., Штрауб Р.Х. Пациенты с рефрактерной болезнью Крона или язвенным колитом реагируют на дегидроэпиандростерон: пилотное исследование. Алимент Фармакол Тер . 2003;17(3):409-414.
2003;17(3):409-414.
Arlt W, Callies F, van Vlijmen JC, et al. Заместительная терапия дегидроэпиандростероном у женщин с надпочечниковой недостаточностью. N Английский J Med . 1999;341(14)-1013-1020.
Barad DH, Gleicher N. Увеличение производства ооцитов после лечения дегидроэпиандростероном. Fertil Steril . 2005;84(3):756.
Барнхарт К.Т., Фриман Э., Гриссо Дж.А. Влияние добавок дегидроэпиандростерона на женщин в перименопаузе с симптомами на эндокринные профили сыворотки, параметры липидов и качество жизни, связанное со здоровьем. J Clin Endocrinol Metab . 1999;84(11):3896-3902.
Барри Н.Н., Макгуайр Д.Л., ван Волленховен РФ. Дегидроэпиандростерон при системной красной волчанке: взаимосвязь между дозировкой, уровнями в сыворотке и клиническим ответом. J Ревматол . 1998;25(12):2352-2356.
Больё ЕЕ. Томас Г., Легрен С. и др. Дегидроэпиандростерон (ДГЭА), сульфат ДГЭА и старение: вклад исследования DHEAge в социобиомедицинскую проблему. Proc Natl Acad Sci USA . 2000;97(8):4279-4284.
Proc Natl Acad Sci USA . 2000;97(8):4279-4284.
Bloch M, Ish-Shalom S, Greenman Y, Klein E, Latzer Y. Влияние лечения дегидроэпиандростероном на вес, плотность костей, метаболизм костей и настроение у женщин, страдающих нервной анорексией — экспериментальное исследование. Психиатрия Рез . 2012; 200(2-3):544-549.
Broeder CE, Quindry MS, Brittingham K, et al. Проект Андро: Физиологическое и гормональное влияние добавок андростендиона на мужчин в возрасте от 35 до 65 лет, участвующих в программе высокоинтенсивных тренировок с отягощениями. Arch Intern Med . 160(20):3093-3104.
Корриган АБ. Дегидроэпиандростерон и спорт. [Обзор]. Med J Aust . 1999;171(4):206-208.
de la Torre B, Hedman M, Befrits R. Уровни сульфата дегидроэпиандростерона в крови и тканях и их связь с хроническим воспалительным заболеванием кишечника. Клин Эксперт Ревматол . 1998;16(5):579-582.
Дайнер Т.С., Ланг В., Геага Дж. и др. Открытое исследование переносимости и фармакокинетики перорального дегидроэпиандростерона с повышением дозы у пациентов с ВИЧ-инфекцией. J Приобретенный иммунодефицитный синдром . 1993;6(5):459-465.
Открытое исследование переносимости и фармакокинетики перорального дегидроэпиандростерона с повышением дозы у пациентов с ВИЧ-инфекцией. J Приобретенный иммунодефицитный синдром . 1993;6(5):459-465.
Финк А., Бернер И.С., Обри-Розье Б., Со А.К. Рандомизированное контролируемое исследование дегидроэпиандростерона у женщин в постменопаузе с фибромиалгией. J Ревматол . 2005;32(7):1336-1340.
Флинн М.А., Уивер-Остергольц Д., Шарп-Тиммс К.Л., Аллен С., Краузе Г. Замена дегидроэпиандростерона у стареющих людей. J Clin Endocrinol Metabol . 199;84(5):1527-1533.
Дженеззани А.Д., Стомати М., Струкки С., Пуччетти С., Луизи С., Дженаццани А.Р. Пероральный прием дегидроэпиандростерона модулирует спонтанную секрецию гормона роста и секреции инсулиноподобного фактора роста-1 у женщин в ранней и поздней постменопаузе. Fertil Steril . 2001;76(2):241-248.
Gomez-Santos C, Hernandez-Morante JJ, Tebar FJ, Granero E, Garaulet M. Дифференциальное влияние перорального дегидроэпиандростерона-сульфата на особенности метаболического синдрома у женщин с ожирением в пре- и постменопаузе.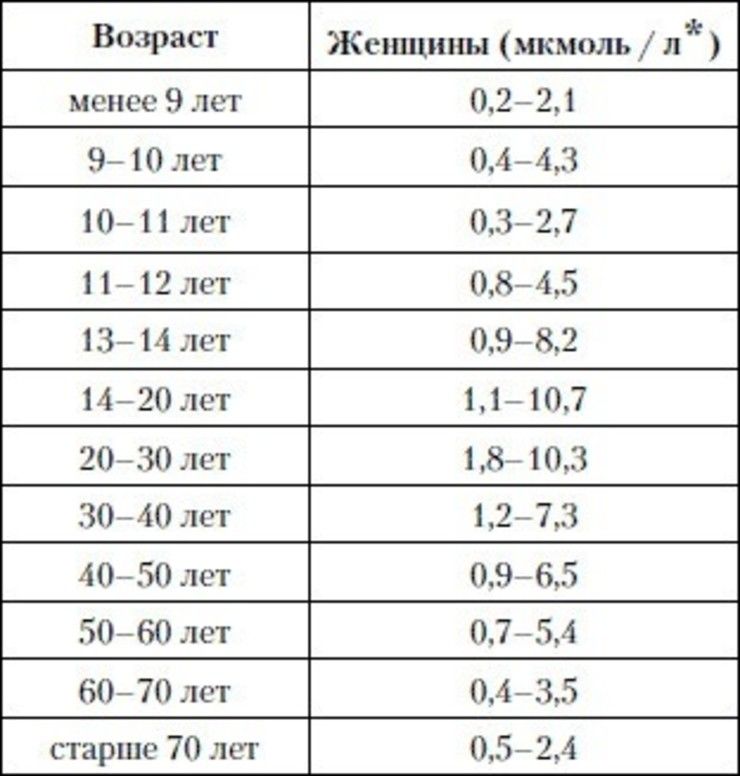 Клин Эндокринол (Oxf) . 2012;77(4):548-554.
Клин Эндокринол (Oxf) . 2012;77(4):548-554.
Гордон С., Грейс Э., Эманс С.Дж., Гудман Э., Кроуфорд М.Х., Лебофф М.С. Изменения маркеров костного обмена и менструальной функции после кратковременного перорального приема ДГЭА у молодых женщин с нервной анорексией. J Шахтер Кости Res . 1999;14(1):136-145.
Гримли Эванс Дж., Малуф Р., Юпперт Ф., ван Никерк Дж.К. Добавка дегидроэпиандростерона (ДГЭА) для улучшения когнитивных функций у здоровых пожилых людей. Кокрановская база данных Syst Rev . 2006; (4): CD006221.
Хансен П.А., Хан Д.Х., Нолте Л.А. ДГЭА защищает от висцерального ожирения и резистентности мышц к инсулину у крыс, получавших диету с высоким содержанием жиров. Am J Physiol . 1997; 273 (5 часть 2): R1704-R1708.
Хинсон Дж.П., Рэйвен П.В. Синдром дефицита ДГЭА: новый термин для старости? [Комментарий]. J Эндокринол . 1999;163(1):1-5.
Klann RC, Holbrook CT, Nyce JW. Химиотерапия мышиной колоректальной карциномы цисплатином и цисплатином плюс 3′-дезокси-3′-азидотимидин. Противораковый рез . 1992;12(3):781-787.
Противораковый рез . 1992;12(3):781-787.
Кохут М.Л., Томпсон Дж.Р., Кэмпбелл Дж. и др. Прием пищевой добавки, содержащей дегидроэпиандростерон (ДГЭА) и андростендион, оказывает минимальное влияние на иммунную функцию у мужчин среднего возраста. J Am Coll Nutr . 2003;22(5):363-371.
Курита Х., Маэсима Х., Кида С. и др. Уровни сывороточного дегидроэпиандростерона (ДГЭА) и ДГЭА-сульфата (S) у пациентов с большим депрессивным расстройством, получавших лекарства, по сравнению с контрольной группой. J Аффективное расстройство . 2013;146(2):205-212.
Лабри Ф. ДГЭА в качестве физиологической заместительной терапии при менопаузе. J Эндокринол Инвест . 1998;21(6):399-401.
Labrie F, Diamond P, Cusan L, Gomez J-L, Belanger A, Candas B. Влияние 12-месячной заместительной терапии дегидроэпиандростероном на кости, влагалище и эндометрий у женщин в постменопаузе. J Clin Endocrinol Metab . 1997;82(10):3498-3505.
Легрен С. , Жирар Л. Фармакология и терапевтические эффекты дегидроэпиандростерона у пожилых людей. Лекарства от старения . 2003;20(13):949-967.
, Жирар Л. Фармакология и терапевтические эффекты дегидроэпиандростерона у пожилых людей. Лекарства от старения . 2003;20(13):949-967.
Либе Р., Барбетта Л., Далл’Аста С. и др. Влияние добавок дегидроэпиандростерона (ДГЭА) на гормональный, метаболический и поведенческий статус у пациентов с гипоадренализмом. J Эндокринол Инвест . 2004;27(8):736-741.
Мельхиор КЛ, Ритцманн РФ. Дегидроэпиандростерон усиливает снотворное и гипотермическое действие этанола и пентобарбитала. Pharmacol Biochem Behav . 1992;43(1):223-227.
Meno-Tetang GML, Hon YY, Jusko WJ. Синергическое взаимодействие между дегидроэпиандростероном и преднизолоном в ингибировании пролиферации лимфоцитов крысы. Иммунофармакол Иммунотоксикол . 1996;18(3):443-456.
Моффат С.Д., Зондерман А.Б., Харман С.М. и др. Взаимосвязь между продольным снижением концентрации дегидроэпиандростерона сульфата и когнитивными способностями у пожилых мужчин. Arch Intern Med . 2000;160(14):2193-2198.
2000;160(14):2193-2198.
Мортола Дж.Ф., Йен С.С. Влияние перорального дегидроэпиандростерона на эндокринно-метаболические параметры у женщин в постменопаузе. J Clin Endocrinol Metab . 1990;71(3)696-704.
Наир К.С., Рицца Р.А., О’Брайен П. и др. ДГЭА у пожилых женщин и ДГЭА или тестостерон у пожилых мужчин. N Английский J Med . 2006;355(16):1647-1659.
Нарквичан А., Маалуф В., Кэмпбелл Б.К., Джаяпракасан К. Эффективность дегидроэпиандростерона для улучшения ответа яичников у женщин с уменьшенным овариальным резервом: метаанализ. Репрод Биол Эндокринол . 2013;11:44.
Nestler JE, Barlascini CO, Clore JN, Blackard WG. Дегидроэпиандростерон снижает уровень липопротеинов низкой плотности в сыворотке крови, а жировые отложения не изменяют чувствительность к инсулину у нормальных мужчин. J Clin Endocrinol Metab . 1988;66(1):57-61.
Nordmark G, Bengtsson C, Larsson A, Karlsson FA, Sturfelt G, Ronnblom L. Влияние добавки дегидроэпиандростерона на качество жизни, связанное со здоровьем, у женщин, получавших глюкокортикоиды, с системной красной волчанкой. Аутоиммунитет . 2005;38(7):531-540.
Аутоиммунитет . 2005;38(7):531-540.
Панджари М., Белл Р.Дж., Джейн Ф., Адамс Дж., Морроу С., Дэвис С.Р. Безопасность 52-недельной пероральной терапии ДГЭА для женщин в постменопаузе. Зрелость . 2009;63(3):240-245.
Панджари М., Дэвис С.Р. Терапия ДГЭА для женщин: влияние на сексуальную функцию и самочувствие. Обновление воспроизведения шума . 2007;13(3):239-248.
Percheron G, Hogrel JY, Denot-Ledunois S, et al. Влияние перорального приема дегидроэпиандростерона в течение 1 года у лиц в возрасте от 60 до 80 лет на мышечную функцию и площадь поперечного сечения: двойное слепое плацебо-контролируемое исследование. Arch Intern Med . 2003;163(6):720-727.
Пикетти С., Джейл Д., Леплеж А. и др. Двойное слепое плацебо-контролируемое исследование перорального дегидроэпиандростерона у пациентов с прогрессирующим заболеванием ВИЧ. Клин Эндокринол (Oxf) . 2001;55(3):325-330.
Порецкий Л., Сонг Л., Brillon DJ и др. Метаболические и гормональные эффекты перорального приема ДГЭА у женщин в пременопаузе с ВИЧ-инфекцией: рандомизированное проспективное плацебо-контролируемое пилотное исследование. Горм Метаб Рез . 2009;41(3):244-249.
Метаболические и гормональные эффекты перорального приема ДГЭА у женщин в пременопаузе с ВИЧ-инфекцией: рандомизированное проспективное плацебо-контролируемое пилотное исследование. Горм Метаб Рез . 2009;41(3):244-249.
Ракель Д., изд. Интегративная медицина . 3-е изд. Филадельфия, Пенсильвания: Эльзевир Сондерс; 2012.
Reiter WJ, Pycha A, Schatzl G, et al. Дегидроэпиандростерон в лечении эректильной дисфункции: проспективное двойное слепое рандомизированное плацебо-контролируемое исследование. Урология . 1999;53(3):590-595.
Sawalha AH, Kovats S. Дегидроэпиандростерон при системной красной волчанке. Curr Rheumatool Rep . 2008;10(4):286-291.
Schifitto G. Вегетативная функция и уровни сульфата дегидроэпиандростерона у ВИЧ-1 инфицированных лиц; отношение к цитокиновому профилю Th2 и Th3. Архнейрол . 2000;57(7):1027-1032.
Столл Б.А. Обзор: Пищевые добавки дейдроэпиандростерона в связи с риском рака молочной железы. Гайка EUR J Clin . 1999;53(10):771-775.
Гайка EUR J Clin . 1999;53(10):771-775.
Тан RS, Пу SJ. Андропауза и потеря памяти: есть ли связь между снижением уровня андрогенов и деменцией у стареющих мужчин? Азиатский J Androl . 2001;3(3):169-174.
Vallee M, Mayo W, Le Moal M. Роль прегненолона, дегидроэпиандростерона и их сульфатных эфиров в обучении и памяти при когнитивном старении. Мозг Res Rev . 2001;37(1-3):301-312.
Ван Волленховен РФ. Дегидроэпиандростерон для лечения системной красной волчанки. Экспертное заключение фармацевта . 2002;3(1):23-31.
Ван Волленховен РФ, Морабито Л.М., Энглеман Э.Г., МакГуайр Д.Л. Лечение системной красной волчанки дегидроэпиандростероном: 50 пациентов лечились до 12 месяцев. J Ревматол . 1998;25(2):285-289.
Вильяреал Д.Т., Холлоши Д.О. Влияние ДГЭА на абдоминальный жир и действие инсулина у пожилых женщин и мужчин: рандомизированное контролируемое исследование. ЯМА . 2004;292(18):2243-2248.
Вознесенский М., Уолш С., Даузер Д., Бриндизи Дж., Кенни А.М. Связь между дегидроэпиандостероном и слабостью у пожилых мужчин и женщин. Возраст Старение . 2009;38(4):401-406.
Вегхофер А., Ким А., Барад Д.Х., Глейхер Н. Влияние метаболизма андрогенов и генотипов FMR1 на потенциал беременности у женщин, принимающих добавки дегидроэпиандростерона (ДГЭА). Hum Reprod . 2012;27(11):3287-3293.
Вайс Э.П., Шах К., Фонтана Л., Ламберт С.П., Холлоши Д.О., Вильярреал Д.Т. Заместительная терапия дегидроэпиандростероном у пожилых людей: 1-й и 2-й эффекты на кости. Am J Clin Nutr . 2009;89(5):1459-1467.
Вайс Э.П., Виллареал Д.Т., Эхсани А.А., Фонтана Л., Холлоши Д.О. Заместительная терапия дегидроэпиандростероном у пожилых людей улучшает показатели жесткости артерий. Ячейка старения . 2012;11(5):876-884.
Уильямс младший. Влияние дегидроэпиандростерона на канцерогенез, ожирение, иммунную систему и старение. Липиды . 2000;35(3):325-331.
2000;35(3):325-331.
Волковиц О.М., Реус В.И., Киблер А. и др. Двойное слепое лечение большой депрессии дегидроэпиандростероном. Am J Психиатрия . 1999;156(4):646-649.
Ян Дж., Шварц А., Хендерсон Э.Е. Ингибирование 3′-аксидо-3′-дезокситимидин-резистентной инфекции ВИЧ-1 дегидроэпиандростероном in vitro. Biochem Biophys Res Commun . 1994;201(3):1424-1432.
Йен ССК, Моралес А.Дж., Хоррам О. Замена ДГЭА у стареющих мужчин и женщин. Возможные лечебные эффекты. Ann NY Acad Sci . 1995; 774:128-142.
Интегрин α2β1, нацеленный на липосомальный доксорубицин, модифицированный DGEA, повышает противоопухолевую эффективность против рака молочной железы
. 2021 5 июля; 18 (7): 2634-2646.
doi: 10.1021/acs.molpharmaceut.1c00132.
Epub 2021 16 июня.
Бинцзе Чжоу
1
, Мин Ли
1
, Сяоминь Сюй
1
, Лань Ян
1
, Мэйлин Е
1
, Ян Чен
1
, Цзяи Пэн
1
, Линьюй Сяо
1
, Луяо Ван
1
, Шици Хуан
1
, Лин Чжан
2
, Цин Линь
1
, Чжижун Чжан
1
Принадлежности
- 1 Ключевая лаборатория системы таргетинга и доставки лекарств Министерства образования и провинции Сычуань, Сычуаньская инженерная лаборатория лекарственных средств растительного происхождения и Сычуаньский исследовательский центр точных промышленных технологий, Западно-китайская школа фармации, Сычуаньский университет, Чэнду 610041, КНР.

- 2 Колледж науки и инженерии полимеров, Сычуаньский университет, Чэнду 610065, КНР.
PMID:
34134485
DOI:
10.1021/acs.molpharmaceut.1c00132
Бинцзе Чжоу и др.
Мол Фарм.
.
. 2021 5 июля; 18 (7): 2634-2646.
doi: 10.1021/acs.molpharmaceut.1c00132.
Epub 2021 16 июня.
Авторы
Бинцзе Чжоу
1
, Мин Ли
1
, Сяоминь Сюй
1
, Лань Ян
1
, Мэйлин Е
1
, Ян Чен
1
, Цзяи Пэн
1
, Линьюй Сяо
1
, Луяо Ван
1
, Шици Хуан
1
, Лин Чжан
2
, Цин Линь
1
, Чжижун Чжан
1
Принадлежности
- 1 Ключевая лаборатория системы таргетинга и доставки лекарств Министерства образования и провинции Сычуань, Сычуаньская инженерная лаборатория лекарственных средств растительного происхождения и Сычуаньский исследовательский центр точных промышленных технологий, Западно-китайская школа фармации, Сычуаньский университет, Чэнду 610041, КНР.

- 2 Колледж науки и инженерии полимеров, Сычуаньский университет, Чэнду 610065, КНР.
PMID:
34134485
DOI:
10.1021/acs.molpharmaceut.1c00132
Абстрактный
Рак молочной железы был основной причиной впервые диагностированных случаев опухолей в 2020 году, занимая второе место среди причин женской смертности. Химиотерапия остается традиционным методом выбора при опухолях молочной железы в большинстве клинических случаев. Однако оно часто сопровождается неблагоприятным прогнозом и тяжелыми побочными эффектами, возникающими в результате недостаточного накопления препарата в опухолевых очагах и бессистемного распределения препарата по организму. Вдохновленный тем фактом, что клетки опухоли молочной железы сверхэкспрессируют интегрин α 2 β 1 на поверхности, мы разработали и сконструировали платформу интегрина α 2 β 1 , нацеленную на модифицированный DGEA липосомальный доксорубицин (DGEA-Lipo-DOX) для применения в терапии рака молочной железы. DGEA-Lipo-DOX был стабильным с однородным размером частиц 121,1 ± 3,8 нм и удовлетворительной инкапсуляцией лекарственного средства. Продемонстрированные in vitro и in vivo , сконструированная платформа показала улучшенную противоопухолевую способность. DGEA-Lipo-DOX показал 4-кратное усиление кровообращения и 6-кратное увеличение накопления DOX в местах опухоли по сравнению со свободным DOX, что привело к значительному повышению противоопухолевой эффективности у мышей с опухолями. Предварительная оценка безопасности показала, что системная токсичность DOX была уменьшена введением DGEA-Lipo. В совокупности связывание интегрина α 2 β 1 DGEA может представлять собой альтернативную терапевтическую стратегию для потенциально более безопасного лечения рака молочной железы.
Вдохновленный тем фактом, что клетки опухоли молочной железы сверхэкспрессируют интегрин α 2 β 1 на поверхности, мы разработали и сконструировали платформу интегрина α 2 β 1 , нацеленную на модифицированный DGEA липосомальный доксорубицин (DGEA-Lipo-DOX) для применения в терапии рака молочной железы. DGEA-Lipo-DOX был стабильным с однородным размером частиц 121,1 ± 3,8 нм и удовлетворительной инкапсуляцией лекарственного средства. Продемонстрированные in vitro и in vivo , сконструированная платформа показала улучшенную противоопухолевую способность. DGEA-Lipo-DOX показал 4-кратное усиление кровообращения и 6-кратное увеличение накопления DOX в местах опухоли по сравнению со свободным DOX, что привело к значительному повышению противоопухолевой эффективности у мышей с опухолями. Предварительная оценка безопасности показала, что системная токсичность DOX была уменьшена введением DGEA-Lipo. В совокупности связывание интегрина α 2 β 1 DGEA может представлять собой альтернативную терапевтическую стратегию для потенциально более безопасного лечения рака молочной железы.
Ключевые слова:
ДГЭА; рак молочной железы; доксорубицин; интегрин α2β1; липосома.
Похожие статьи
Повышенная противоопухолевая и антиметастазная эффективность против агрессивного рака молочной железы с липосомальным доксорубицином, нацеленным на фибронектин.
Цзян К., Сун Х., Ян Л., Ли Л., Ван З., Сунь Х., Гонг Т., Линь К., Чжан З.
Цзян К. и др.
J Управление выпуском. 2018 10 фев; 271:21-30. doi: 10.1016/j.jconrel.2017.12.026. Epub 2017 23 декабря.
J Управление выпуском. 2018.PMID: 29277681
Улучшение доставки лекарственного средства и противоопухолевой эффективности пегилированного липосомального доксорубицина путем нацеливания на РНК-аптамеры у мышей с моделью опухоли молочной железы.

Moosavian SA, Abnous K, Badiee A, Jaafari MR.
Моосавиан С.А. и др.
Коллоиды Surf B Биоинтерфейсы. 2016 1 марта; 139: 228-36. doi: 10.1016/j.colsurfb.2015.12.009. Epub 2015 15 декабря.
Коллоиды Surf B Биоинтерфейсы. 2016.PMID: 26722819
Надежный, воздействующий на опухоль и чувствительный к окислительно-восстановительному потенциалу полимерсомальный доксорубицин: превосходная альтернатива Доксилу и Кэликсу?
Цзоу И, Мэн Ф, Дэн С, Чжун З.
Цзоу Ю и др.
J Управление выпуском. 2016 10 октября; 239: 149-58. doi: 10.1016/j.jconrel.2016.08.022. Epub 2016 25 августа.
J Управление выпуском. 2016.PMID: 27569664
Направленный GE11 функциональный полимерный доксорубицин как усовершенствованная альтернатива клиническому липосомальному составу для лечения рака яичников.

Цзоу И, Ся И, Мэн Ф, Чжан Дж, Чжун З.
Цзоу Ю и др.
Мол Фарм. 4 сентября 2018 г .; 15 (9): 3664-3671. doi: 10.1021/acs.molpharmaceut.8b00024. Epub 2018 2 апр.
Мол Фарм. 2018.PMID: 29570299
Углубленное проникновение в клеточный/субклеточный интерфейс и повышенная противоопухолевая эффективность нанопрепаратов, декорированных циклическим пептидным лигандом, ускоряющих действие активных целевых нанопрепаратов.
Ши NQ, Ли Ю, Чжан Ю, Ли ZQ, Ци XR.
Ши Н.К. и др.
Int J Наномедицина. 2018 19 сентября; 13: 5537-5559. doi: 10.2147/IJN.S172556. Электронная коллекция 2018.
Int J Наномедицина. 2018.PMID: 30271146
Бесплатная статья ЧВК.
Посмотреть все похожие статьи
Цитируется
Терапевтическое подавление mTOR с помощью системно введенных нейтральных липосомальных наночастиц, нагруженных миРНК, ингибирует DMBA-индуцированный канцерогенез молочной железы.

Саху Р., Джха С., Паттанаяк С.П.
Саху Р. и др.
Бр Дж Рак. 2022 г., 19 октября. doi: 10.1038/s41416-022-02011-1. Онлайн перед печатью.
Бр Дж Рак. 2022.PMID: 36261586
Ориентация на интегрины для лечения рака — разочарования и возможности.
Бергонзини К., Крозе К., Цвимер А.Дж.М., Данен Э.Х.Дж.
Бергонзини С. и др.
Front Cell Dev Biol. 2022 9 марта; 10:863850. doi: 10.3389/fcell.2022.863850. Электронная коллекция 2022.
Front Cell Dev Biol. 2022.PMID: 35356286
Бесплатная статья ЧВК.Обзор.
Достижения в области нанолипосом для диагностики и лечения рака печени.
Ли И, Чжан Р, Сюй З, Ван З.
Ли Ю и др.
Int J Наномедицина. 2022 26 февраля; 17: 909-925. doi: 10.



 Он резко падает после рождения и затем возрастает при половом созревании. Пика концентрация ДЭА-SO4 достигает после полового созревания, затем она уменьшается с возрастом.
Он резко падает после рождения и затем возрастает при половом созревании. Пика концентрация ДЭА-SO4 достигает после полового созревания, затем она уменьшается с возрастом.



Leave a Reply